Bimbel.Co.Id – Pengertian Atom adalah unit dasar dari segala materi di alam semesta ini. Meskipun sangat kecil, atom adalah “bata dasar” dari segala sesuatu yang kita lihat, sentuh, dan rasakan di sekitar kita. Mari kita mulai dengan mendefinisikan apa itu atom dan bagaimana konsep ini telah berkembang dari masa ke masa. Dalam artikel ini, kita akan menyelami lebih dalam mengenai struktur, sifat, dan peran atom dalam kehidupan sehari-hari.
Pengertian Atom
Atom adalah unit terkecil dari suatu unsur yang masih mempertahankan sifat-sifat kimianya. Sejarah pengertian atom dimulai sejak zaman kuno, tetapi pemahaman modern tentang atom dimulai pada abad ke-19 dan ke-20. Salah satu tokoh penting dalam pengembangan konsep atom adalah John Dalton, seorang ilmuwan Inggris yang mengemukakan model atom yang pertama.
Sejarah Perkembangan Atom
Atom adalah salah satu konsep paling mendasar dalam ilmu pengetahuan, dan perkembangannya telah melibatkan kontribusi dari banyak ilmuwan terkemuka sepanjang sejarah. Mari kita telusuri sejarah perkembangan atom dari masa ke masa.
Zaman Kuno dan Konsep Filosofis
Pemikiran tentang atom sudah muncul sejak zaman kuno di berbagai budaya, seperti di Yunani kuno dengan tokoh-tokoh seperti Demokritos dan Leucippus. Mereka mengemukakan gagasan tentang “atomos”, yaitu partikel-partikel yang tidak dapat dibagi lagi.
Abad Pertengahan dan Konsep Alkimia
Pada abad pertengahan, konsep atom masih berkembang dalam konteks alkimia. Para alkimia memperkenalkan gagasan tentang elemen-elemen dasar dan transformasi materi, meskipun tidak selalu sesuai dengan pemahaman modern tentang atom.
Abad Ke-18: Awal Mula Kimia Modern
Pada abad ke-18, ilmu kimia mulai berkembang sebagai ilmu yang terpisah dari alkimia. Pada masa ini, teori atom kembali muncul dengan lebih kuat melalui kontribusi-kontribusi dari ilmuwan seperti John Dalton.
Teori Dalton tentang Atom
Pada tahun 1808, John Dalton memperkenalkan teori atom modern yang menyatakan bahwa atom adalah partikel terkecil dari unsur yang masih mempertahankan sifat-sifat kimianya. Teori ini memberikan landasan bagi pemahaman modern tentang atom.
Abad Ke-19: Pengembangan Lebih Lanjut
Pada abad ke-19, pemahaman tentang atom terus berkembang. Dmitri Mendeleev mengembangkan tabel periodik unsur, yang mengorganisir unsur-unsur berdasarkan sifat-sifat kimianya dan menunjukkan pola periodik dalam sifat-sifat tersebut.
Abad Ke-20: Era Atom
Abad ke-20 ditandai dengan perkembangan besar dalam pemahaman tentang atom. Eksperimen Rutherford menemukan bahwa atom memiliki inti yang padat yang dielilingi oleh elektron yang bergerak mengelilinginya, menggantikan model atom yang homogen.
Teori Atom Quantum
Pada pertengahan abad ke-20, teori atom quantum dikembangkan, yang menggambarkan sifat-sifat atom menggunakan prinsip-prinsip mekanika kuantum. Kontribusi dari ilmuwan seperti Niels Bohr, Erwin Schrödinger, dan Werner Heisenberg memperkaya pemahaman kita tentang atom.
Era Modern dan Penemuan Terbaru
Di era modern, penelitian tentang atom terus berlanjut dengan pesat. Penemuan baru seperti partikel subatom dan penggunaan teknologi nuklir menunjukkan betapa pentingnya pemahaman tentang atom dalam konteks dunia modern.
Pengertian Atom Menurut Para Ahli
Atom adalah salah satu konsep paling mendasar dalam ilmu pengetahuan, dan para ahli telah memberikan berbagai definisi tentang apa itu atom sepanjang sejarah. Mari kita telusuri pengertian atom menurut pandangan beberapa ahli terkemuka.
Demokritos: Atomos
Demokritos, seorang filsuf Yunani kuno, dikenal sebagai salah satu tokoh pertama yang mengemukakan konsep pengertian atom. Baginya, atom adalah bagian terkecil dari materi yang tidak dapat dibagi lagi dan membentuk segala sesuatu di alam semesta. Dia menyebut partikel-partikel ini sebagai “atomos”, yang berarti “tidak dapat dibagi”.
John Dalton: Partikel Terkecil Unsur
John Dalton, seorang ilmuwan Inggris pada abad ke-19, merumuskan teori pengertian atom modern. Menurut Dalton, atom adalah partikel terkecil dari suatu unsur yang masih mempertahankan sifat-sifat kimianya. Dia juga menyatakan bahwa atom tidak dapat diciptakan atau dihancurkan dalam reaksi kimia.
Niels Bohr: Model Atom
Niels Bohr, seorang fisikawan Denmark pada awal abad ke-20, mengembangkan model pengertian atom yang lebih rinci. Menurut Bohr, atom terdiri dari inti yang terdiri dari proton dan neutron, di sekitarnya elektron bergerak dalam lintasan terdefinisi. Model ini membawa konsep kuantum ke dalam pemahaman kita tentang atom.
Erwin Schrödinger: Persamaan Gelombang
Erwin Schrödinger, seorang fisikawan Austria, memberikan kontribusi besar dalam pengembangan teori pengertian atom quantum. Melalui persamaan gelombang Schrödinger, ia menggambarkan perilaku elektron dalam atom sebagai gelombang probabilitas, bukan partikel yang bergerak dengan jalur tertentu.
Werner Heisenberg: Prinsip Ketidakpastian
Werner Heisenberg, seorang fisikawan Jerman, mengemukakan prinsip ketidakpastian, yang menyatakan bahwa kita tidak dapat secara tepat menentukan posisi dan momentum suatu partikel subatom secara bersamaan. Prinsip ini memiliki implikasi besar dalam pemahaman kita tentang struktur atom.
Sifat-Sifat Atom
Atom adalah unit dasar dari materi dan memiliki berbagai sifat yang menentukan perilaku dan interaksi mereka dalam berbagai situasi. Mari kita telusuri beberapa sifat-sifat penting dari atom.
Ukuran Atom
Atom memiliki ukuran yang sangat kecil, bahkan dibandingkan dengan ukuran mikroskopis lainnya. Radius atom umumnya berkisar dari 0,1 hingga 0,5 nanometer (nm), atau sekitar 1 hingga 5 angstrom (Å). Ini berarti bahwa atom sangat sulit untuk diamati langsung dengan mata telanjang atau bahkan dengan mikroskop biasa.
Massa Atom
Massa atom diukur dalam satuan massa atom (u) atau dalton (Da). Sebagian besar disumbangkan oleh proton dan neutron di inti atom, sedangkan massa elektron sangat kecil dibandingkan dengan keduanya. Massa atom bervariasi tergantung pada jumlah proton dan neutron di inti atom.
Muatan Atom
Atom terdiri dari proton, neutron, dan elektron. Proton bermuatan positif, neutron netral, dan elektron bermuatan negatif. Jumlah proton dalam inti atom menentukan muatan positif bersih atom, yang seimbang dengan jumlah elektron yang mengelilingi inti atom.
Isotop
Isotop adalah atom dari unsur yang sama yang memiliki jumlah proton yang sama tetapi jumlah neutron yang berbeda di inti atomnya. Ini berarti bahwa isotop dari suatu unsur memiliki sifat kimia yang sama, tetapi massa atomnya berbeda. Contoh isotop yang umum adalah isotop hidrogen: hidrogen, deuterium, dan tritium.
Kestabilan Atom
Kestabilan atom ditentukan oleh rasio antara proton dan neutron di inti atom. Atom yang memiliki jumlah proton dan neutron yang seimbang cenderung lebih stabil, sementara atom yang memiliki rasio yang tidak seimbang mungkin menjadi tidak stabil dan mengalami peluruhan radioaktif.
Sifat Kimia Atom
Sifat kimia atom ditentukan oleh konfigurasi elektron di sekitar inti atom. Elektron yang mengisi lapisan terluar atom menentukan bagaimana atom berinteraksi dengan atom lain dalam reaksi kimia. Konfigurasi elektron ini juga memengaruhi sifat fisik atom, seperti konduktivitas listrik dan panas.
Reaktivitas Atom
Reaktivitas atom adalah kemampuan atom untuk berpartisipasi dalam reaksi kimia dengan atom lain. Atom dengan lapisan terluar yang belum sepenuhnya terisi cenderung lebih reaktif karena mereka cenderung mencapai konfigurasi elektron yang lebih stabil dengan berbagi atau mentransfer elektron.
Keteraturan Periodik
Tabel periodik unsur menggambarkan keteraturan dalam sifat-sifat atom, seperti muatan, ukuran, dan reaktivitas. Pola periodik ini menggambarkan tren dalam sifat-sifat atom yang bergantung pada jumlah proton dalam inti atom.
Ciri-Ciri Atom
Atom, sebagai unit dasar dari materi, memiliki sejumlah ciri-ciri yang menentukan sifat dan perilaku mereka. Mari kita jelajahi beberapa ciri-ciri utama dari atom.
1. Terdiri dari Proton, Neutron, dan Elektron
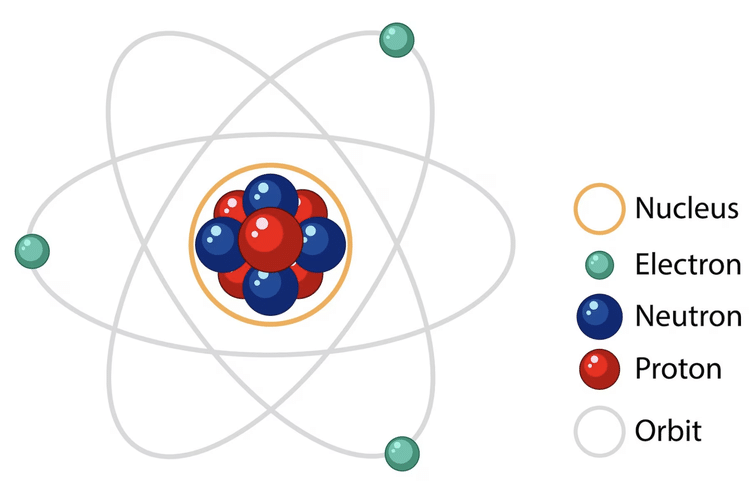
Atom terdiri dari tiga jenis partikel utama: proton, neutron, dan elektron. Proton bermuatan positif dan terletak di inti atom bersama neutron yang netral. Elektron bermuatan negatif dan bergerak mengelilingi inti atom dalam lintasan yang disebut lapisan elektron.
2. Ukuran yang Sangat Kecil
Ukuran atom sangat kecil, bahkan dibandingkan dengan benda-benda mikroskopis lainnya. Atom memiliki radius sekitar 0,1 hingga 0,5 nanometer (nm), atau sekitar 1 hingga 5 angstrom (Å). Kecilnya ukuran atom membuatnya sulit untuk diamati langsung dengan mata telanjang.
3. Atom Lebih Banyak Ruang Kosong
Meskipun atom memiliki struktur yang padat, sebagian besar ruang di dalam atom adalah ruang kosong. Inti atom yang terdiri dari proton dan neutron hanya membentuk sebagian kecil dari volume total atom, sedangkan sebagian besar volume diisi oleh area di mana elektron bergerak.
4. Atom Bervariasi dalam Massa dan Muatan
Massa atom diukur dalam satuan massa atom (u) atau dalton (Da). Massa atom sebagian besar ditentukan oleh jumlah proton dan neutron di inti atom. Atom juga memiliki muatan listrik yang bervariasi, tergantung pada jumlah proton dan elektron di dalamnya.
5. Atom dapat Membentuk Ikatan Kimia
Atom memiliki kemampuan untuk berinteraksi dengan atom lain dan membentuk ikatan kimia. Ikatan ini terjadi ketika atom saling berbagi atau mentransfer elektron, membentuk molekul atau senyawa kimia baru.
6. Atom Tidak Stabil dapat Mengalami Peluruhan Radioaktif
Beberapa atom dapat menjadi tidak stabil dan mengalami peluruhan radioaktif. Hal ini terjadi ketika inti atom tidak seimbang, misalnya memiliki terlalu banyak neutron atau proton. Peluruhan ini menghasilkan emisi partikel atau energi yang dapat berubah menjadi bentuk yang lebih stabil.
7. Atom memiliki Sifat-Sifat Periodik
Atom menunjukkan pola periodik dalam sifat-sifat mereka dalam tabel periodik unsur. Pola ini menggambarkan tren dalam sifat-sifat atom yang bergantung pada jumlah proton dalam inti atom, seperti muatan, ukuran, dan reaktivitas.
Komponen-Komponen Atom
Atom, sebagai unit dasar dari materi, terdiri dari beberapa komponen utama yang membentuk struktur dan sifatnya. Mari kita jelajahi komponen-komponen tersebut.
1. Proton
Proton adalah salah satu komponen utama dari atom. Ini memiliki muatan positif dan terletak di inti atom bersama dengan neutron. Jumlah proton dalam inti atom menentukan identitas unsur kimia dari atom tersebut.
2. Neutron
Neutron adalah partikel netral yang juga terdapat di dalam inti atom bersama dengan proton. Juga tidak memiliki muatan listrik, sehingga berperan dalam menstabilkan inti atom dengan menyeimbangkan gaya tolak antar proton di dalamnya.
3. Elektron
Elektron adalah partikel yang memiliki muatan negatif dan bergerak mengelilingi inti atom dalam lapisan elektron. Ini memiliki massa yang sangat kecil di bandingkan dengan proton dan neutron, dan jumlah elektron di sekitar inti atom menentukan sifat kimia dari atom tersebut.
4. Inti Atom
Inti atom terdiri dari proton dan neutron yang terikat bersama dalam struktur yang padat. Yakni salah satu bagian terpadat dari atom dan membentuk sebagian kecil dari total volume atom. Inti atom mengandung sebagian besar massa atom dan menentukan identitas unsur kimia dari atom tersebut.
5. Lapisan Elektron
Lapisan elektron adalah area di sekitar inti atom di mana elektron bergerak. Ini dalam atom di atur dalam lapisan-lapisan yang di sebut kulit elektron atau orbital. Jumlah dan susunan elektron dalam lapisan ini menentukan sifat fisik dan kimia dari atom tersebut.
6. Ruang Kosong
Meskipun atom memiliki struktur yang padat, sebagian besar volume atom di isi oleh ruang kosong. Inti atom hanya membentuk sebagian kecil dari total volume atom, sementara sebagian besar ruang di isi oleh area di mana elektron bergerak.
7. Elektron Valensi
Elektron valensi adalah elektron yang terletak di lapisan terluar atom. Ini berperan dalam menentukan sifat kimia atom dan kemampuannya untuk berikatan dengan atom lain. Juga memengaruhi konduktivitas listrik dan panas dari suatu zat.
Manfaat Atom
Atom, sebagai unit dasar dari materi, memiliki berbagai manfaat dalam berbagai bidang kehidupan manusia. Mari kita jelajahi beberapa manfaat utama dari atom:
1. Energi Nuklir
Atom memiliki potensi besar sebagai sumber energi melalui reaksi nuklir. Energi nuklir di hasilkan dari pembelahan inti atom (fisi nuklir) atau penggabungan inti atom (fusi nuklir). Pembangkit listrik tenaga nuklir menggunakan reaksi fisi nuklir untuk menghasilkan energi listrik yang bersih dan efisien.
2. Pengobatan Radiasi
Teknologi atom di gunakan dalam pengobatan radiasi, seperti dalam terapi radiasi untuk mengobati kanker. Radiasi ionisasi dari radioisotop di gunakan untuk menghancurkan sel kanker atau mencegah pertumbuhan sel kanker yang tidak di inginkan dalam tubuh.
3. Pengujian Bahan
Atom di gunakan dalam teknik pengujian bahan seperti spektroskopi atom dan analisis aktivasi neutron. Metode ini memungkinkan ilmuwan untuk menganalisis komposisi kimia dan struktur material dengan akurasi tinggi, penting dalam pengembangan material baru dan pemahaman sifat-sifatnya.
4. Penandaan Isotop
Isotop atom di gunakan dalam penandaan isotop untuk melacak pergerakan dan proses dalam berbagai sistem biologis dan lingkungan. Aplikasi ini di gunakan dalam penelitian ilmiah, bidang kedokteran, dan industri untuk mempelajari proses-proses kompleks dalam berbagai sistem.
5. Pertanian dan Pangan
Atom di gunakan dalam bidang pertanian dan pangan, seperti dalam teknik penstrerilan menggunakan radiasi, penggunaan radioisotop dalam penelitian pertanian, dan pemantauan keamanan pangan menggunakan teknik penandaan isotop. Ini membantu meningkatkan produktivitas pertanian dan keamanan pangan.
6. Pemantauan Lingkungan
Isotop atom di gunakan dalam pemantauan lingkungan untuk melacak pergerakan polutan, sumber air, dan proses alami seperti siklus air dan sedimentasi. Aplikasi ini membantu dalam pemahaman dan perlindungan lingkungan alam kita.
Contoh Atom
Atom adalah unit dasar dari materi dan merupakan komponen utama dari segala sesuatu di alam semesta ini. Berikut adalah beberapa contoh-contoh atom dari unsur yang berbeda:
1. Hidrogen (H)
Hidrogen adalah unsur kimia yang paling sederhana dan paling melimpah di alam semesta. Atom hidrogen terdiri dari satu proton di inti atom dan satu elektron yang mengelilingi inti atom. Contoh-contoh hidrogen dapat di temukan dalam air (H2O), gas hidrogen (H2), dan berbagai senyawa organik.
2. Karbon (C)
Karbon adalah unsur yang penting dalam kimia organik dan merupakan dasar bagi kehidupan di Bumi. Atom karbon memiliki enam proton di inti atom dan berbagai susunan elektron di sekitarnya. Contoh-contoh karbon dapat di temukan dalam berbagai senyawa organik, seperti karbohidrat, lipid, dan protein.
3. Oksigen (O)
Oksigen adalah unsur yang sangat penting untuk kehidupan manusia dan proses-proses biologis di Bumi. Atom oksigen memiliki delapan proton di inti atom dan berbagai susunan elektron di sekitarnya. Contoh-contoh oksigen dapat di temukan dalam air (H2O), udara yang kita hirup (O2), dan dalam berbagai senyawa anorganik dan organik.
4. Besi (Fe)
Besi adalah logam yang umum di gunakan dalam berbagai aplikasi industri dan konstruksi. Atom besi memiliki 26 proton di inti atom dan berbagai susunan elektron di sekitarnya. Contoh-contoh besi dapat di temukan dalam bahan bangunan, kendaraan, alat-alat rumah tangga, dan banyak lagi.
5. Emas (Au)
Emas adalah logam yang langka dan sangat di hargai karena kilauannya dan ketahanannya terhadap korosi. Atom emas memiliki 79 proton di inti atom dan berbagai susunan elektron di sekitarnya. Contoh-contoh emas dapat di temukan dalam perhiasan, perangkat elektronik, dan dalam aplikasi industri khusus.
6. Uranium (U)
Uranium adalah unsur radioaktif yang penting dalam produksi energi nuklir dan aplikasi medis. Atom uranium memiliki 92 proton di inti atom dan berbagai susunan elektron di sekitarnya. Contoh-contoh uranium dapat di temukan dalam bahan bakar nuklir, senjata nuklir, dan dalam penelitian ilmiah.
Kesimpulan
Pemahaman tentang atom sangat penting dalam ilmu pengetahuan modern. Atom bukan hanya unit dasar dari materi, tetapi juga kunci untuk memahami fenomena alam dan perkembangan teknologi. Dengan terus melakukan penelitian dan eksplorasi tentang atom, kita dapat membuka lebih banyak wawasan tentang alam semesta ini.
FAQs
- Apakah pengertian atom itu benar-benar tak terlihat?
- Bagaimana penemuan partikel subatom mengubah pandangan kita tentang atom?
- Apa implikasi dari penemuan isotop dalam kimia modern?
- Mengapa penting untuk mempelajari struktur atom?
- Apa saja potensi risiko dari teknologi yang melibatkan atom?